Тема уроку: Білки
актуалізувати знання про білки з курсу біології;
вивчити фізичні і хімічні властивості, кольорові реакції білків;
учні повинні вміти характеризувати склад і будова білків,
функції білків в клітині, значення їх для життя.
Устаткування і реактиви: концентрована HNO3. білок, розчини CuSO4. NaOH, спиртівка, сірники, тримач, пробірки.
Білки, за твердженням Ф. Енгельса, одна з форм існування життя.
"Всюди, де ми зустрічаємо життя, ми знаходимо, що вона пов'язана з яким-небудь білковим тілом, і всюди, де ми зустрічаємо якесь білкове тіло, яке не знаходиться в процесі розкладання, ми без винятку читаємо і явище життя". (К. Маркс, Ф. Енгельс. Зібрання творів. Т. 20). Білки - будівельний матеріал, виконують рухову, каталітичну, транспортну, захисну, енергетичну функції.
Білки були виділені в окремий клас біологічних молекул в XVIII столітті в результаті робіт французького хіміка Антуана Фуркруа та інших вчених, в яких було зазначено властивість білків коагулювати (денатурувати) під впливом нагрівання або кислот. У той час були досліджені такі білки, як альбумін ( "яєчний білок"), фібрин (білок з крові) і глютен із зерна пшениці.
У 80-х роках XIX століття російський біохімік Данилевський А.Я. трохи пізніше - (в 1903 р) німецький вчений Фішер Е. - висунули полипептидную теорію будови білків: білки з'єднані в ланцюжок із залишків # 945; - амінокислот за допомогою пептидних зв'язків # 8213; СО # 8213; NH # 8213 ;.
В даний час відомо 22 амінокислоти, які і створюють безліч білкових молекул. Причому кожна з них має свій, строго певний, порядок чергування амінокислот. Виділяють чотири структури білкової молекули. Первинна - чергування залишків # 945; - амінокислот; вторинна - ланцюги, закручені у вигляді спіралі; третинна - конфігурація, яку приймає в просторі закручена спіраль (вона забезпечує біологічну активність білкової молекули); четвертичная - з'єднані один з одним макромолекули білків. При нагріванні, струшуванні руйнується третинна структура білка, він втрачає свою біологічну дію.
Білки - це складні високомолекулярні природні сполуки, побудовані із залишків # 945; - амінокислот, сполучених пептидними (амідних) зв'язками # 8213; СО # 8213; NH # 8213 ;.
Число амінокислотних залишків, що входять в молекули білків, по-різному: в інсуліні їх 51 (20 в одній і 31 - в інший ланцюжку), в миоглобине - 140. Молекулярні маси білків можуть коливатися від 10 000 до кількох мільйонів.
Mr (білка яйця) = 36 000; Mr (білка м'язів) = 1 500 000. Склад гемоглобіну виражається формулою (C738 H1166 O208 N203 S2 Fe) 4. Порахувати його молекулярну масу нескладно.
Білки є головним носієм життя. Відомості про склад і будову білків отримані при вивченні продуктів їх гідролізу. В даний час встановлено, що молекули більшості білків складаються з 22 різних # 945; - амінокислот.
До складу білків входять: С - 50 - 52%; Н - 6 - 8%; Про - 19 - 24%; N- 15 - 18%; S- 0,5 - 2,0%.
Сучасні дослідження дозволяють розрізняти в структурі білка первинну, вторинну, третинну і четвертинних структури. (Слайд 6).
Під первинною структурою білка розуміється точна послідовність розташування окремих амінокислотних залишків в макромолекулі (всі зв'язки ковалентні, міцні). С.228 підручника, мал.37.
Вторинна структура - форма поліпептидного ланцюга в просторі (найчастіше спіраль). Білкова ланцюг закручена в спіраль (за рахунок безлічі водневих зв'язків).
Третинна структура - реальна тривимірна конфігурація, що виникає при закручуванні в спіраль поліпептидних ланцюгів білків, що відбувається під дією дисульфідних, водневих та інших зв'язків.
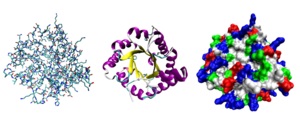
Різні способи зображення тривимірної структури білка.
Четвертичная структура - з'єднання один з одним макромолекул білків. Утворюють комплекс. С.229, рис.40.
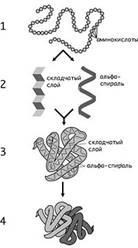
Рівні структури білків: 1 - первинна; 2 - вторинна; 3 - третинна; 4 - четвертинна.
Багато білки (глобулярні) розчинні у воді, розчинах солей, кислот і майже все розчиняються в лугах; не розчиняються в органічних розчинниках; нерозчинні білки (фібрилярні), у тому числі побудовано тканини живих організмів (шкіра, сухожилля, м'язи, нігті, волосся), а білки плазми крові розчинні.
1) гідроліз (при нагріванні з розчинами кислот, лугів, при дії ферментів)
H2N # 8213; CH2 # 8213; C # 8213 ;: N # 8213; CH # 8213; C # 8213 ;: N # 8213; CH # 8213; C = O → H2N # 8213; CH2 # 8213; C = O +
H2O CH2 H2O CH2 OH OH
+ H2N # 8213; CH # 8213; C = O + H2N # 8213; CH # 8213; C = O
Гідроліз білків зводиться до гідролізу поліпептидних зв'язків. До цього ж зводиться і перетравлення білків:
Білок ↔ амінокислоти → кров в усі клітини і тканини організму.
2) денатурація - порушення природної структури білка (під дією нагрівання і хімічних реагентів)
Денатурація білка курячого яйця під впливом високої температури
__________ cвойства кислот
__________ властивості підстав
4) кольорові реакції білків - якісні реакції
Лабораторний досвід. Правила роботи!
а) ксантопротеїнова реакція.
Налийте в пробірку трохи білка. Прилейте до нього 3-4 краплі концентрованої азотної кислоти. Відзначте, що відбулися.
Білок + HNO3 конц. → жовте забарвлення
б) биуретовая реакція.
Налийте в пробірку трохи гідроксиду натрію, додайте до нього розчин сульфату міді (II) так, щоб луг залишалася в надлишку. До отриманого осадку прилейте розчин білка. Відзначте, які відбулися зміни.
Білок + Cu (OH) 2 ↓ → розчин фіолетового кольору.
Як ще можна визначити білок? (При горінні - запах паленого пір'я).
Висновок: якісними на білки є реакції з концентрованою азотною кислотою (жовте забарвлення), з обложеної гідроксидом міді (II) (розчин фіолетового кольору) і горіння білків (запах паленого пір'я).
З органічних сполук, що входять в живу клітину, найважливішу роль відіграють білки. На їх частку припадає близько 50% маси клітини.
Білки є будівельним матеріалом для оболонки, органоїдів і мембран клітини. З них побудовані кровоносні судини, сухожилля, волосся.
Вони виконують каталітичну функцію. Всі клітинні каталізатори - білки (активні центри ферменту), структура активного центру ферменту і структура субстрату точно відповідають один одному.
Скоротливі білки викликають всякий рух.
Білки виконують транспортну роль - білок крові гемоглобін приєднує кисень і розносить по всіх тканинах.
Білки виконують захисну функцію - вироблення білкових тіл антитіл для знешкодження чужорідних речовин.
При розкладанні 1 г білка виділяється 17,6 кДж енергії. (Розкладаються білки до СО2. NH3. Сечовини (NH2) 2 CO і H2 O).
У м'язах - до 80%, в селезінці, крові, легенів - близько 72%, в шкірі - 63%, в печінці - 57%, в мозку - 15%, жирова тканина, кісткова і тканину зубів містять від 14 до 28% білків .
Білки входять до складу багатьох лікарських препаратів. Ведуться роботи по штучному отриманню білкових речовин (синтезовані інсулін, рибонуклеаза).
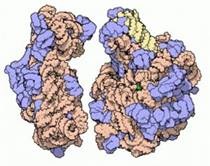
Молекулярна модель малої (зліва) і великий (праворуч) субодиниць бактеріальної рибосоми - молекулярної машини, синтезує білки. Блакитним кольором показані білки в складі рибосоми, але основну структурну роль виконує рРНК.
Це важливо, тому що експерти Всесвітньої організації охорони здоров'я вважають, що приблизно половина населення земної кулі знаходиться в стані білкового голодування, а світова нестача харчового білка становить близько 15 млн. Тонн на рік при нормі споживання білка в добу дорослою людиною 115 грам.
Ми згадали те, що ви знали про білках з курсу біології, розглянули хімічні властивості білків, їх значення для життя. Пропоную вам перевірити ваші минулі знання, відповівши на питання. Вам потрібно вставити пропущені слова або фрази.
Головним носієм життя є ....
... - це складні високомолекулярні сполуки, побудовані з ....
Елементний склад білків: ....
Молекулярна маса білків змінюється від ... до ....
Багато білки розчиняються в ..., майже всі розчиняються в ....
Нерозчинні білки, з яких побудовані ....
У структурі білка розрізняють ... структури.
Функції білків в організмі ....
білки; залишків # 945; - амінокислот.
Десяти тисяч, мільйонів.
Воді, розчинах солей, кислот; лугах.
Тканини живих організмів: шкіра, сухожилля, м'язи, нігті, волосся.
Первинну, вторинну, третинну, четвертичную.
Будівельна, каталітична, рухова, транспортна, захисна, енергетична.
"5" - всі відповіді правильні; "3" - 3 невірних відповіді;
"4" - 1-2 невірних відповіді; "2" - 4 і більше невірних відповідей.
Білки - це складні високомолекулярні природні сполуки, побудовані із залишків # 945; - амінокислот, сполучених пептидними (амідних) зв'язками # 8213; СО # 8213; NH # 8213 ;.
Число амінокислотних залишків, що входять в молекули білків, по-різному: інсулін - 51, міоглобін - 140. Mr (білка) = від 10 000 до кількох мільйонів.
Mr (білка яйця) = 36 000; Mr (білка м'язів) = 1 500 000.
Первинна - послідовність чергування амінокислотних залишків (всі зв'язки ковалентні, міцні).
Вторинна - форма поліпептидного ланцюга в просторі (найчастіше спіраль). Білкова ланцюг закручена в спіраль (за рахунок безлічі водневих зв'язків). Третинна - реальна тривимірна конфігурація, яку приймає в просторі закручена спіраль (за рахунок гідрофобних зв'язків), у деяких S - S - зв'язку (бісульфідні зв'язку).
Четвертичная - з'єднані один з одним макромолекули білків.
1) гідроліз (при нагріванні з розчинами кислот, лугів, при дії ферментів)
H2N # 8213; CH2 # 8213; C # 8213 ;: N # 8213; CH # 8213; C # 8213 ;: N # 8213; CH # 8213; C = O → H2N # 8213; CH2 # 8213; C = O +
H2O CH2 H2O CH2 OH OH
+ H2N # 8213; CH # 8213; C = O + H2N # 8213; CH # 8213; C = O
Гідроліз білків зводиться до гідролізу поліпептидних зв'язків. До цього ж зводиться і перетравлення білків:
білок ↔ амінокислоти → кров в усі клітини і тканини організму.
2) денатурація - порушення природної структури білка (під дією нагрівання і хімічних реагентів)
__________ cвойства кислот
| __________ властивості підстав
4) кольорові реакції білків - якісні реакції
а) ксантопротеїнова реакція.
Білок + HNO3 конц. → жовте забарвлення
б) биуретовая реакція.
Білок + Cu (OH) 2 ↓ → розчин фіолетового кольору.
в) горіння - запах паленого пір'я.
Висновок: якісними на білки є реакції з концентрованою азотною кислотою (жовте забарвлення), з обложеної гідроксидом міді (II) (розчин фіолетового кольору) і горіння білків (запах паленого пір'я).
Роль білків в клітині.
1. Будівельний матеріал - утворення оболонки, органоїдів і мембран клітини. Побудовано кровоносні судини, сухожилля, волосся.
2. Каталітична роль - все клітинні каталізатори білки.
3. Рухова функція - скоротливі білки викликають всякий рух.
4. Транспортна функція - білок крові гемоглобін приєднує кисень і розносить по всіх тканинах.
5. Захисна роль - вироблення білкових тіл антитіл для знешкодження чужорідних речовин.
6. Енергетична роль: 1 г білка → 17,6 кДж.