Щільність аміаку і інші його фізичні властивості
У звичайних умовах аміак являє собою безбарвний газ з різким задушливим запахом. Щільність аміаку дорівнює 0,73 кг / м 3.
Молекула аміаку має хімічний склад, який відбивається формулою NH3. Він має форму тригональной піраміди (dNH = 0,10нм, кут HNH = 107,3 0) (рис. 1). Відповідно до теорії валентних зв'язків це відповідає sp 3-гібридизації валентних орбіталей атома азоту. З чотирьох sp 3 -гібрідних орбіталей азоту три беруть участь в утворенні трьох σ-зв'язків N-H, а четверту орбіталь займає не зв'язуюча електронна пара. У термінах теорії молекулярних орбіталей це відповідає заповнення трьох зв'язують і однієї майже не зв'язує молекулярної σ-орбіталі:
Оскільки не зв'язує двухелектронних хмара орієнтоване в просторі, молекула аміаку - різко виражений донор електронної пари і має високу полярністю (m = 0,49 × 10 -29 Кл × м).
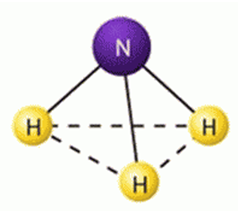
Мал. 1. Будова молекули аміаку.
Полярність зв'язку N-H обумовлює між молекулами аміаку водневу зв'язок. Тому температури плавлення (-77,8 o С) і кипіння (-33,4 o С) аміаку досить високі; він характеризується значною ентальпії випаровування і легко зріджується.
Рідкий аміак, як і вода, - сильно іонізуючий розчинник. При цьому похідні NH4 + в рідкому аміаку поводяться як кислоти (амінокислоти), а похідні NH2 - - як підстави (аммонооснованія). Наприклад, сильними кислотами в рідкому аміаку є NH4 Cl, NH4 NO3. а підставами - KNH2. Ba (NH2) 2. Дігідронітріди Zn (NH2) 2. Al (NH2) 3 поводяться як амфотерні сполуки.
Аміак дуже добре розчиняється у воді (при 20 o С в одному об'ємі води розчиняється близько 700 обсягів аміаку). Хороша розчинність пояснюється утворенням водневого зв'язку між молекулами NH3 і H2 O.
Короткий опис хімічних властивостей і щільність аміаку
Аміак дуже реакционноспособен, схильний до реакцій прісоедіненія.Сгорает в кисні, реагує з кислотами, металами, галогенами, оксидами і галогенидами.
2NH3 + 2Al = 2AlN + 3H2 (вище t = 600 o C).
Якісна реакція на аміак - почорніння папірці, смоченнойраствором Hg2 (NO3) 2 (освіта ртуті). Осушують аміак оксидом кальцію.
Рідкий аміак - основний протонний розчинник; добре растворяетсеру, нітрати (крім фторидів) і нітрати лужних металів, галогенідиаммонія, перманганат калію; погано розчиняє неорганічні фториди, сульфати, карбонати.
Приклади розв'язання задач
Розрахуйте молярну масу газу, щільність якого по повітрю дорівнює 0,756.
Відношення маси даного газу до маси іншого газу, взятого в тому ж обсязі, при тій же температурі і тому ж тиску, називається відносною щільністю першого газу за другим. Дана величина показує, у скільки разів перший газ важчий або легше другого газу.
Відносну молекулярну масу повітря приймають рівною 29 (з урахуванням змісту в повітрі азоту, кисню та інших газів). Слід зазначити, що поняття «відносна молекулярна маса повітря» вживається умовно, так як повітря - це суміш газів.
Dair (gas) = M (gas) / M (air);
M (gas) = M (air) × Dair (gas);
M (gas) = 29 × 0,756 = 22 г / моль.
Молярна маса газу дорівнює 22 г / моль.
Визначте молярну масу невідомого газу, якщо рівні об'єми цього газу і кисню при однакових умовах мають маси 4,15 г і 0,32 м
Відношення маси даного газу до маси іншого газу, взятого в тому ж обсязі, при тій же температурі і тому ж тиску, називається відносною щільністю першого газу за другим. Дана величина показує, у скільки разів перший газ важчий або легше другого газу.
Молярна маса водню дорівнює:
Тоді, молярна маса невідомого газу
M (gas) = M (O2) × DO2 (gas) = 32 × 1,328 = 42,5 г / моль.